La importancia de los voluntarios para la ciencia: cómo sumarse para la fase final de la vacuna argentina contra el COVID
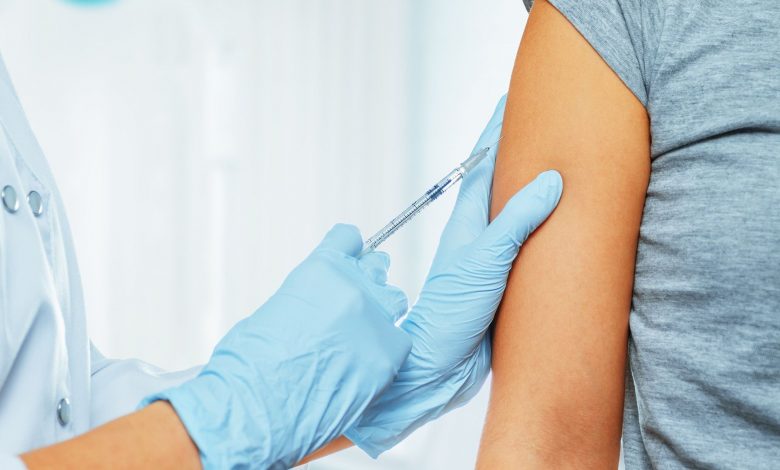

La vacuna argentina ARVAC Cecilia Grierson contra el COVID-19, un desarrollo íntegramente nacional a través de un trabajo mancomunado entre el sistema científico público y privado, ya ingresó en la fase final del ensayo clínico. Tal como informó Infobae a comienzos de marzo, los científicos a cargo del estudio buscan incorporar 1.800 voluntarios a fin de evaluar la seguridad y la inmunogenicidad (el aumento de anticuerpos neutralizantes contra el virus SARS-CoV-2) de la inmunización.
La fórmula nacional se inscribe entre las denominadas vacunas de segunda generación, es decir que será destinada para dosis de refuerzo en personas ya inmunizadas y, además, su principio activo puede actualizarse para eventuales nuevos sublinajes del virus que escapen a la respuesta inmunológica.
En el proceso participaron científicos del CONICET, de la Universidad Nacional de San Martín (UNSAM) y del laboratorio Pablo Cassará.

Para esta etapa los investigadores están reclutando 1.782 voluntarios. Los cuales deben ser personas mayores de 18 años, sin límite de edad. Pueden presentar comorbilidades y el único requisito es haber recibido las dos dosis del esquema inicial contra el COVID-19, de cualquier plataforma, y una dosis más de refuerzo.
Sobre el requerimiento de dosis recibidas para la participación de los voluntarios, Juliana Cassataro, bióloga (UNSAM), doctora en Inmunología y líder del equipo UNSAM-CONICET que trabaja en esta vacuna, señaló en conferencia de prensa que se deben circunscribir a este número inmunizaciones porque “nos tenemos que comparar con otras vacunas del mundo y la mayoría se probaron como refuerzo en individuos que tuvieron esta cantidad de dosis, o menos”.
Al tiempo que resaltó que “este ensayo contempla a mayores de 18 años, pero a todos los que superen esta edad”. Incluso, detalló que, aquellos que se inscriban, deberán aguardar al menos 4 meses desde la última inmunización contra el COVID-19.

Se trata de un estudio de alcance federal, por lo que en esta etapa trabajan 10 sitios de investigación distribuidos en el territorio nacional. Los centros de salud se encuentran en la Ciudad de Buenos Aires, Salta, Córdoba, Mendoza, y Mar del Plata y La Plata, en la provincia de Buenos Aires.
Para ser voluntario, hay que inscribirse en el siguiente enlace.
Durante el estudio de Fase II/III se evaluará la seguridad e inmunogenicidad de tres fórmulas de ARVAC Cecilia Grierson, incluyendo una versión con un antígeno de Ómicron BA.4 y BA.5. “Vamos a probar la dosis monovalente Gamma, monovalente Ómicron y la fórmula bivalente compuesta por estas dos. Se utilizarán estas tres ramas para lograr la comparación final”, dijo a Infobae Cassataro, bióloga (UNSAM) y líder del equipo UNSAM-CONICET.

A partir de los resultados parciales de la Fase I, se obtuvo información de seguridad preliminar que demostró que la vacuna ARVAC Cecilia Grierson es segura y muy inmunogénica. A su vez, se comprobó que una dosis de refuerzo aumenta hasta 30 veces los anticuerpos neutralizantes contra las variantes del virus Ómicron y Gamma.
La Fase II/III de la investigación consta de dos etapas. En la primera, que comenzó a principios de este año y sigue en curso, se administró la vacuna a 232 personas en dos centros de la Ciudad de Buenos Aires, en el CEMIC y Clinical Pharma. Estos participantes, junto a los nuevos convocados, conformarán un grupo de 2.014 voluntarios en total para esta etapa final.
Se espera que entre mayo y junio de este año los resultados sean presentados en la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) para su aprobación por la agencia regulatoria, según anticiparon los investigadores a Infobae durante la presentación de la última etapa de la investigación, que se desarrolló el 6 de marzo pasado en la Universidad Nacional de San Martín (UNSAM).

Es la primera vez que una vacuna contra enfermedades infecciosas diseñada y desarrollada integralmente en Argentina logra completar los estudios clínicos de Fase I y avanzar a Fase II/III. Más de 100 personas entre científicos, técnicos e investigadores integran los equipos que llevaron adelante todas las instancias.
Según adelantaron desde el laboratorio Pablo Cassará, ya cuentan con la capacidad industrial para producir más de 4 millones de dosis mensuales de antígeno vacunal y ya comenzaron su fabricación en paralelo al desarrollo de los estudios de Fase II/III.
En esta última instancia se incorporó al equipo de trabajo el doctor e investigador Gonzalo Pérez Marc, quien junto al doctor Fernando Polack y su equipo, realizó el primer estudio en suelo nacional sobre la vacuna contra el COVID-19 de Pfizer.

“La idea es desarrollar la Fase III a gran escala y en poco tiempo para, si los resultados son buenos, tener la vacuna lo antes posible”, señaló Pérez Marc a Infobae y agregó: “Armamos una red con 10 centros con investigadores que tienen mucha experiencia trabajando con nosotros. Somos un equipo de médicos y médicas que nos formamos haciendo investigación a gran escala, que es un tipo de investigación clínica muy particular, requiere grandes volúmenes pero con el mismo nivel de calidad que si lo hiciéramos con un solo voluntario”.
Un grupo de voluntarios recibirá una dosis de vacuna y otra de placebo, “lo que buscamos es evaluar si el ascenso de anticuerpos neutralizantes es similar a lo que se observó en Fase I y que la seguridad sea tan buena como se vio en Fase I y en lo que llevamos de Fase II. Si eso sucede, estaríamos en condiciones de presentar los resultados a la ANMAT”, dijo Pérez Marc y estimó que la fórmula ARVAC Cecilia Grierson podría ser aprobada para mitad de este año .
“El perfil de seguridad de la vacuna es excelente, no hemos visto ningún evento adverso, y en cuanto al ascenso de anticuerpos, el aumento para proteger tanto para el virus ancestral del SARS-CoV-2 de Wuhan como para Gamma y Ómicron, son muy buenos tanto como la de cualquier vacuna internacional”, completó Pérez Marc a este medio.

Este proyecto comenzó con el financiamiento inicial de la Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación (Agencia I+D+i) del Ministerio de Ciencia y Tecnología de la Nación, y continuó con la inversión del Laboratorio Cassará en el desarrollo tecnológico y en los estudios de Fase I.
“No es un proyecto de investigación que no sabemos cuándo va a entrar en producción, ya estamos produciendo el antígeno de la vacuna, en paralelo a la investigación clínica. Para que el día que esté autorizada, tengamos millones para distribuir”, precisó a Infobae Jorge Cassará, licenciado en Química y directivo del laboratorio que participa del desarrollo y realizará la producción.
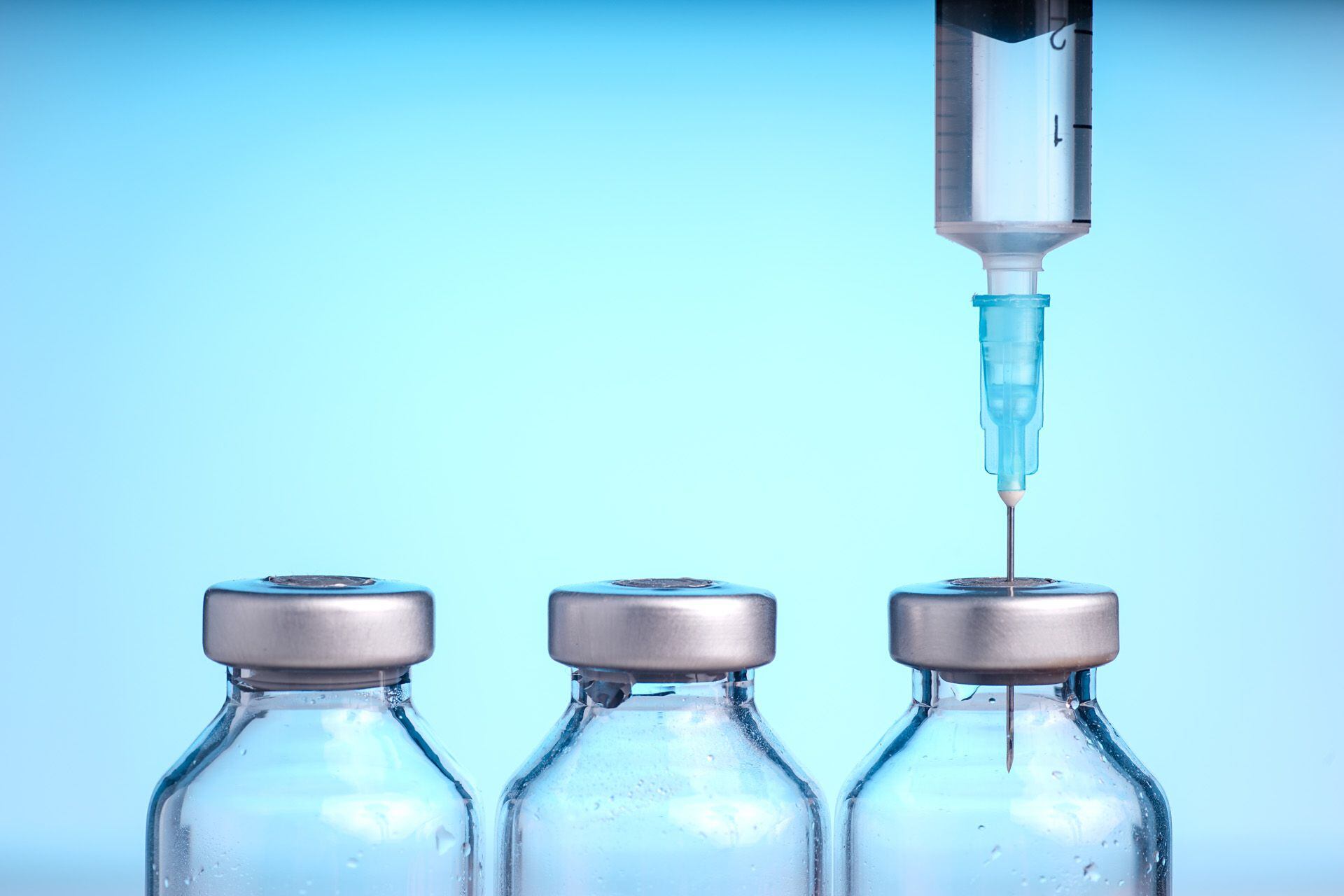
La vacuna ARVAC Cecilia Grierson se basa en la tecnología de proteínas recombinantes , una plataforma segura que ya se aplica en las vacunas contra la Hepatitis B en niños recién nacidos desde hace más de 20 años o más recientemente, el VPH (virus del papiloma humano).
Durante el proceso tecnológico a escala industrial de ARVAC, que comenzó en el año 2021, se desarrollaron 5 tecnologías de producción de antígeno en las variantes del SARS-CoV-2 Wuhan, Gamma, Delta, Ómicron B1 y Ómicron BA.4 y BA.5. En el estudio de Fase I se comprobó que la fórmula es segura y que incrementa hasta 30 veces los anticuerpos neutralizantes contra Wuhan, Gamma y Ómicron.

Las dosis podrán ser almacenadas entre 2 y 8°C en heladera, lo que permitirá que las vacunas ARVAC Cecilia Grierson, a diferencia de los primeros inoculantes contra el COVID-19, sean más económicas, fáciles de producir y de distribuir.
Entre las ventajas comparativas del inoculante argentino, Cassataro enumeró: “Por un lado, es un tipo de plataforma muy conocida, que puede ser producida en nuestro país desde cero y en todas sus etapas, hasta el envasado. Además, puede ser guardada en heladera, algo que también baja el costo de distribución en un país tan grande como nuestro”.
Este tipo de tecnología (producto basado en proteínas recombinantes) se guarda en la heladera y puede conservarse por un año; por lo tanto, para la distribución en lugares remotos donde no tienen acceso a un freezer de -70 es sustancial.
Seguir leyendo:
Vacuna argentina ARVAC Cecilia Grierson: buscan 1.800 voluntarios para la fase final de investigación
“Para ayudar al avance de la ciencia”: 7 de cada 10 argentinos afirmó que sería voluntario en estudios clínicos
La vacuna bivalente hecha 100% en la Argentina comenzará el lunes con el proceso de la Fase II/III
La vacuna bivalente argentina ARVAC contra el COVID avanza a paso firme y promete frenar a Ómicron y sus subvariantes
La ANMAT autorizó la Fase II/III de la vacuna bivalente argentina ARVAC contra el coronavirus: cuándo comienzan los ensayos clínicos

